2.2. Vznik spektra
Princip:
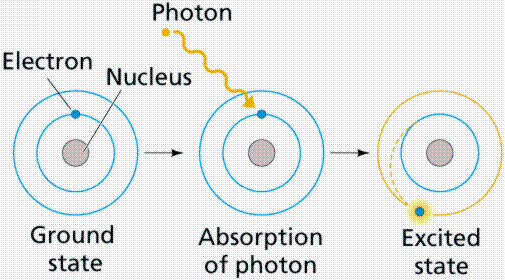
Přivedením elektronu do tzv.
vybuzeného stavu, tj. dodáním větší množství energie, než mu přísluší v jeho
základním stavu (termicky, opticky, nebo elektricky) dojde k jeho přeskoku
na energeticky bohatší hladinu a po krátké prodlevě k jeho návratu do
původního stavu. Tím se dříve přijatá energie uvolní ve formě záření o určité
frekvenci (vlnové délce). Vlnová délka vyzářené energie je pro každý prvek
charakteristická a je kvalitativní charakteristikou záření.
Energie fotonu: ∆E
= Eq – Ep = h . n = h . c / λ
n … kmitočet záření
h … Planckova konstanta
(6,625 .10-34 J.s)
c … rychlost záření (3
Ztráta energie je doprovázena emisí záření a vlnové
délky jsou určeny horní a spodní energetickou hladinou přechodu:
λ
= c . h / Eq – Ep
λ … vlnová délka záření (nm)
Pravděpodobnost přechodu atomu z excitovaného
stavu do stavu s nižší energií není u různých přechodů stejná.
Uvažujeme-li existenci pouze dvou stavů atomů (základní
I10
≈ konst. A10
. N1
I10 … intenzita emisní čáry pro přechod 1→0
Návrat
valenčního elektronu na základní hladinu atomu je spojen s emisí záření,
které se neprojevuje jediným přechodem, ale řadou postupných dovolených
přechodů => pozorujeme více čar ve vzniklém spektru.
Složitost
spekter a počet čar roste u prvků od první k osmé skupině periodické
tabulky